1. Введение
Антитела, возможно, являются одним из наиболее важных компонентов “инструментария” молекулярного биолога. Они произвели революцию в биологических исследованиях и теперь оказывают свое влияние в клинике как эффективные терапевтические средства. После знакомства со структурой и типами антител, а также с технологией рекомбинантных антител, в этой главе подробно описаны свойства рекомбинантных антител REAfinity ™ и их использование в проточной цитометрии.
1.1. Структура
Антитела характеризуются своей уникальной формой “Y”. Каждое антитело состоит из четырех полипептидов — двух тяжелых цепей и двух легких цепей. По своим функциональным характеристикам в структуре можно выделить вариабельные и константные области. Вариабельная область, состоящая из N-терминальных концов тяжелых и легких цепей, содержит сайт связывания антигена. Константная область, которая состоит из оставшейся части молекул, определяет иммунный ответ или механизм, используемый для разрушения антигенов (рис. 1).
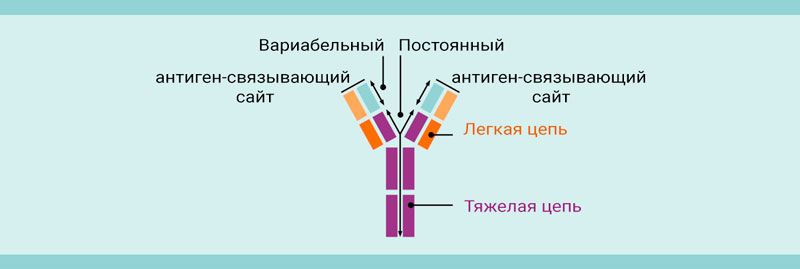
Рисунок 1. Иллюстрация структуры антитела.
Антитело состоит из четырех полипептидов — двух тяжелых цепей и двух легких цепей. По своим функциональным характеристикам эти цепи содержат в своей структуре вариабельные и постоянные области. Вариабельная область содержит сайт связывания антигена.
Каждое антитело может быть протеолитически расщеплено на три фрагмента – два фрагмента Fab и фрагмент Fc. Fab, сокращение для связывания фрагмента с антигеном, включает вариабельные концы антитела. Фрагмент Fc, сокращение для кристаллизуемого фрагмента, определяет биологические эффекторные функции антитела, такие как антитело-зависимая клеточная цитотоксичность (ADCC) и комплемент-зависимая цитотоксичность (CDC). В ADCC Fc-фрагмент антитела связывается с Fc-рецепторами (FcγR) на поверхности лейкоцитов, что приводит к фагоцитозу или лизису клеток-мишеней. В CDC антитела запускают каскад комплемента на клеточной поверхности, что приводит к гибели клеток.
1.2. Классификация изотипов антител
Антитела делятся на пять основных изотипов в зависимости от их структуры, биологических свойств и способности бороться с антигенами. В таблице 1 приведены изотипы и их свойства, распределение и иммунные функции. (Janeway, E.A. et al. (2001). Распределение и функции изотипов иммуноглобулинов. Иммунобиология. Иммунная система в здоровье и болезни. 5-е изд.)
Большинство антител для анализа относятся к подклассу IgG, который подразделяется на четыре изотипа: IgG1, IgG2, IgG3 и IgG4 у людей и IgG1, IgG2a, IgG2b и IgG3 у мышей. Изоформы IgG проявляют разные уровни эффекторных функций — уровень эффекторной функции ADCC высок для человеческого IgG1 и IgG3, низок для IgG2 и IgG4, тогда как уровень эффекторной функции CDC высок для человеческого IgG1 и IgG3, низок для IgG2 и нулевой для IgG4.
Таблица 1. Изотипы
| Изотип | Субкласс | Структура | Главная иммунная функция | Распределение |
| IgA | IgA1 и IgA2 | Мономер, димер | Нейтрализация | Внеклеточная жидкость (мономерный IgA), секреция через эпителий как в случае грудного молока (димерный IgA) |
| IgD | Мономер | Функция не ясна | В основном связан с B-клетками | |
| IgE | Мономер | Активация тучных клеток | Тучные клетки под поверхностями эпителия (а именно, дыхательных путей, желудочно-кишечного тракта и кожи) | |
| IgG | IgG 1-4 (в человеке) | Мономер | Нейтрализация, опсонизация, активация системы комплемента, подготовка к цитотоксической функции NK-клеток | Плазма, внеклеточная жидкость |
| IgM | Пентамер | Активация системы комплемента | Плазма, экстраваскулярные пространства |
1.3. Классификация (первичные и вторичные антитела)
Антитела, которые связываются со специфическими антигенами, представляющими интерес, помогают биологам визуализировать различные биологические объекты — от белков на мембране вестерн-блота до клеточных и внутриклеточных структур.
Первичные антитела связываются напрямую с антигеном. В зависимости от типа эксперимента, первичные антитела используются отдельно или в комбинации с вторичным антителом. Например, в проточной цитометрии первичные (конъюгированные с флуорохромами) почти всегда используются в одиночку, тогда как в микроскопии комбинация первичных антител со вторичными используется для усиления сигнала.
Вторичные антитела помогают обнаруживать, сортировать или очищать интересующие антигены путем связывания с первичным антителом. Они образуются видоспецифически и против изотипа первичного антитела. Например, для первичного антитела, полученного из кролика, было бы достаточно вторичного антитела (против кроличьих антител), полученного у хозяина, отличного от кролика. Первичные антитела часто являются изотипами IgG и, следовательно, потребуются вторичные антитела против IgG. Вторичные антитела часто конъюгированы с ферментами, красителями или флуоресцентными белками. Выбор здесь зависит от типа эксперимента; например, в экспериментах по иммунофлюоресценции вторичные антитела, конъюгированные с флуоресцентными белками или красителями, являются правильным выбором.
Система с двумя антителами — первичная-вторичная система — часто используется для:
- более сильной локализации красителя на антигене,
- многоцветного окрашивания в образце и в экспериментах с использованием одного первичного антитела и нескольких вторичных антител с флуоресцентной меткой,
- по экономическим причинам.
1.4. Поликлональные в сравнении с моноклональными антителами
Поликлональные антитела (pAbs) представляют собой гетерогенную смесь антител, продуцируемых различными клонами B-лимфоцитов. Они в основном состоят из смеси подтипов IgG и распознают множественные эпитопы антигена. Сыворотка поликлональных антител может быть получена в течение 4–8 недель путем инъекции подопытному животному интересующего антигена с последующим наблюдением ответа и сбором антисыворотки. Их производство недорого по сравнению с моноклональными антителами. (PMID: 15953834)
Моноклональные антитела (mAb) продуцируются одним клоном B-лимфоцитов и распознают только определенный эпитоп на антигене. Они состоят только из одного подтипа. Эти mAb продуцируются гибридомами, т.е. В-клетками, иммортализованными слиянием с клетками миеломы (рис. 2). (PMID: 15728446)
По сравнению с поликлональными антителами, производство моноклональных антител более сложное, дорогое и занимает много времени (3–6 месяцев). (PMID: 15953834)
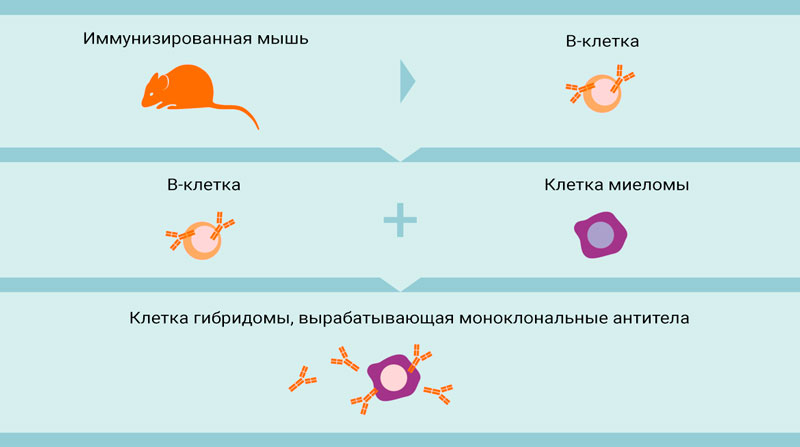
Рисунок 2. Стандартная технология гибридомы для получения моноклональных антител.
Моноклональные антитела (mAb) продуцируются одним клоном B-лимфоцитов и распознают только определенный эпитоп на антигене. Они состоят только из одного подтипа антител. Эти моноклональные антитела продуцируются гибридомами, то есть В-клетками, иммортализованными путем слияния с клетками миеломы.
Полученные из гибридомы моноклональные антитела часто загрязнены примесями из двух источников: легких цепей иммуноглобулинов, полученных из миеломы, и иммуноглобулинов класса G (IgG), полученных из сыворотки. (PMID: 29485921) Эти примеси снижают специфичность , что приводит к непредсказуемым результатам (рис. 3).
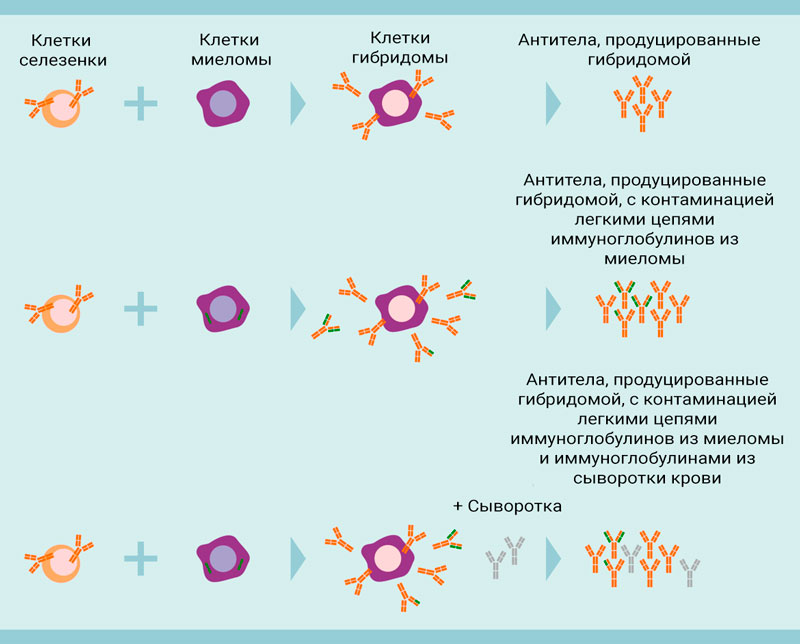
Рисунок 3. Моноклональные антитела, полученные из гибридомы, теряют чистоту.
Моноклональные антитела, полученные из гибридомы, часто загрязнены примесями из легких цепей IgG (источник: миелома), и иммуноглобулинами IgG из сыворотки.
1.5. Кризис воспроизводимости в исследованиях в области наук о живом: антитела являются основными обвиняемыми
Непредсказуемость результатов является основной проблемой, стоящей сегодня перед научным сообществом. Несколько факторов способствуют этой сложной проблеме. Согласно Второму ежегодному отчету о состоянии трансляционных исследований за 2014 год, проведенному корпорацией Sigma-Aldrich по вопросу предсказуемости и воспроизводимости, антитела были одним из основных классов продуктов, вносящих вклад в проблему (около 36%), и вторым после моделей животных (около 41%). Согласно еще одному исследованию, проведенному Американским обществом клеточной биологии в 2014 году, и опросу членов данного общества, 50% респондентов назвали реагенты, включая антитела, сыворотку и плазмиды, причиной неудачи предсказуемости и воспроизводимости экспериментов.
Воспроизводимость, связанная с антителами, может быть улучшена путем соблюдения следующих рекомендаций всеми вовлеченными сторонами — поставщиками, пользователями и журналами:
- Валидация антител для конкретного применения
- Прозрачная и четкая отчетность об использовании реагентов
- Продажа и использование однородных по качеству антител
Одним из решений является использование антител, полученных с помощью технологии рекомбинантных антител. (PMID: 25652980) Рекомбинантные антитела проявляют более высокую чистоту, согласованность между партиями и определимость благодаря стандартизированным системам клеточных культур и доступности последовательности ДНК по сравнению с моноклональными антителами, полученными из гибридомы.
2. Технология рекомбинантных антител
Рекомбинантные антитела (rAb) представляют собой моноклональные антитела, генерируемые in vitro (и без использования животных) посредством технологии рекомбинантных ДНК. Рекомбинантные антитела преодолевают многие ограничения, свойственные обычным моноклональным (см. Таблицу 2). (PMID: 26482034)
Таблица 2. Рекомбинантные антитела превосходят традиционные моноклональные.
| Преимущества технологии рекомбинантных антител | |
| Высокая аффинность
|
Рекомбинантные антитела могут быть сконструированы, чтобы иметь аффинность от пикомолярного до фемтомолярного диапазона |
| Высокая специфичность | Рекомбинантные антитела могут быть сконструированы таким образом, чтобы находить различие между похожими антигенами-мишенями |
| Разнообразие мишеней | Мишени рекомбинантных антител включают в себя образцы ткани, целые клетки, маленькие молекулы, специфические конформации белков, трансмембранные белки, РНК, посттрансляционные модификации, и комплексы, такие как биотинилированные комплексы главного комплекса гистосовместимости с пептидом |
| Независимость от иммунного ответа | Рекомбинантные антитела могут быть получены против нестабильных, токсичных, летучих, иммуносупрессивных, или неиммуногенных антигенов |
| Уменьшенная иммуногенность | Терапевтические рекомбинантные антитела человека вызывают иммунный ответ сравнимый с антителами животных |
| Многосторонность | Генерация полноразмерных антител или меньших фрагментов, подобно моновалентным или бивалентным Fab-фрагментам, и переключение изотипа, используя простые техники клонирования, являются возможными |
| Более быстрое получение | Автоматизированное высокопроизводительное производство; как только библиотека антител наработана, производство рекомбинантных антител займет приблизительно от 2-ух до 8-ми недель, в то время как в животных весь процесс займет более 4 месяцев |
| Надежность | В отличие от клеточных линий гибридомы, запасы рекомбинантных антител не имеют риска вымирания |
| Более высокая воспроизводимость | Поскольку последовательности рекомбинантных антител известны, они более надежны и дают более воспроизводимые результаты, чем моноклональные антитела |
| Низкая вариабельность между партиями | Стандартизированное производство рекомбинантных антител приводит к низкой вариабельности между различными партиями антител |
| Производство без животных | Животные не используются, если только иммунные библиотеки антител не получены из животных |
2.1. Рекомбинантные антитела: способы получения
Процесс производства рекомбинантных антител состоит из следующих этапов:
- Определение последовательности интересующих генов, кодирующих антитела
- Синтез генов и клонирование в экспрессионные векторы
- Экспрессия фрагментов антител в клетках млекопитающих или бактерий
- Очистка и анализ
Для получения рекомбинантных антител часто используются стабильные клеточные линии, такие как CHO и HEK293.
Фрагменты антител для наработки рекомбинантных антител могут быть получены из существующих моноклональных антител или могут быть выбраны из библиотек генов (кодирующих немного разные белки антител) в соответствии со сродством антител к связыванию с антигенами-мишенями. Основанные на библиотеке способы получения рекомбинантных антител подразделяются на дисплейные платформы in vitro, такие как фаговый дисплей и рибосомный дисплей, и дисплейные платформы in vivo, такие как бактериальный, дрожжевой и млекопитающий дисплей на клеточной поверхности. На рисунке 4 ниже представлены основные вехи производства рекомбинантных антител. (PMID: 15953834, 4001944, 3140379, 3045807, 3210233, 2247164, 8248129, 9181578, 16763048)
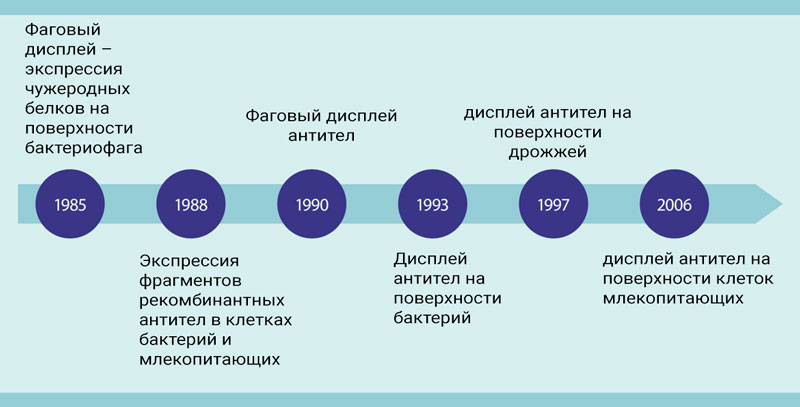
Фаговый дисплей является наиболее распространенным методом, который включает следующие шаги:
- Конструкция библиотеки: Фрагменты гена, кодирующие тяжелую и легкую цепи антитела, клонируют в фаговые векторы, что приводит к фаговой библиотеке, экспонирующей антитела с различными сайтами связывания антигена.
- Отбор с помощью пэннинга: Пэннинг — это процесс, при котором антитела отбираются путем инкубации фаговой библиотеки с антигеном-мишенью, иммобилизованным на твердой поверхности. Несвязанные фаговые частицы вымываются, а связанные фаги элюируются и размножаются в E.coli.
- Клонирование и отбор: Полученные ДНК антител клонируют в векторы экспрессии и экспрессируют в E.coli.
- Скрининг и созревание аффинности: Чтобы улучшить аффинность антитела, в выбранные молекулы антитела вводят разнообразные последовательности такими способами, как склонная к ошибкам ПЦР или сайт-направленный мутагенез. Антитела оценивают на улучшенную аффинность, и из выбранных клонов экспрессируют и очищают.
3. REAfinity ™ Антитела: рекомбинантные антитела для проточной цитометрии
REAfinity ™ рекомбинантные антитела — это новое поколение рекомбинантно генерируемых антител, специально разработанных для применения проточной цитометрии. Они обеспечивают превосходные постоянство и чистоту от партии к партии по сравнению с моноклональными антителами мыши или крысы. Следующие структурные особенности антител REAfinity делают их лучшим выбором антител для экспериментов с использованием проточной цитометрии (рис. 5).
- Универсальный изотип IgG человека снижает сложность планирования эксперимента, устраняя необходимость включения нескольких контролей изотипа во время анализа данных проточной цитометрии.
- Мутированная область Fc устраняет фоновые сигналы, устраняя любое связывание рекомбинантно сконструированных антител с FcγR.
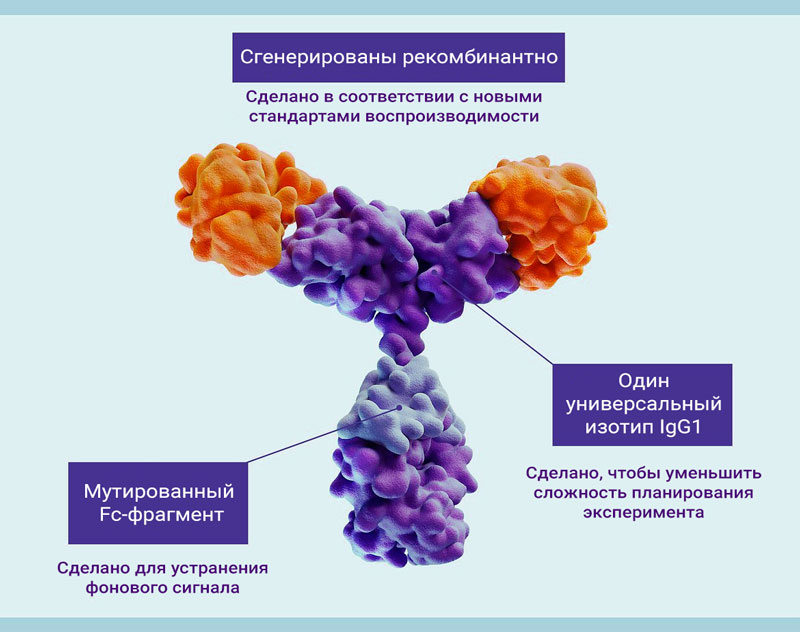
Рисунок 5: Структурные особенности REAfinity антител.
3.1. REAfinity рекомбинантные антитела: производственный процесс
Антитела REAfinity получают путем клонирования антигенсвязывающей области из традиционного моноклонального антитела (мышиный IgG), полученного из гибридомы, с Fc-областью человеческого IgG1. Область Fc мутируется, чтобы устранить связывание рекомбинантных антител с рецепторами Fcγ. Эта химерная ДНК экспрессируется в клеточной линии млекопитающих, культивируемой в стандартизированных бессывороточных условиях. Для обеспечения согласованности между партиями используется одна и та же клеточная линия для производства всех антител REAfinity (рис. 6).
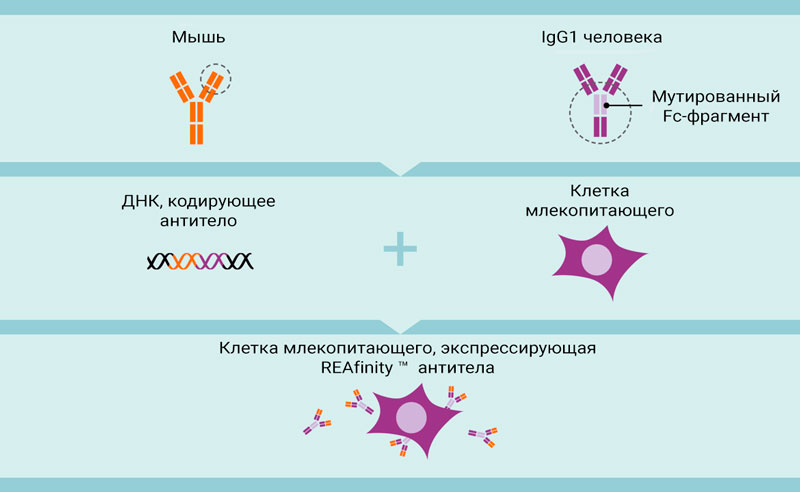
Рис.6. Технологический процесс производства REAfinity.
Преимущества этого метода производства включают в себя:
- Отсутствие примесей легких цепей из-за четко определенной химерной последовательности IgG
- Отсутствие примесей, происходящих из клеток, так как клетки запрограммированы исключительно для экспрессии определенного антитела
- Отсутствие сывороточных примесей, так как клетки млекопитающих культивируются в бессывороточных средах
3.2. REAfinity рекомбинантные антитела: уникальные особенности и преимущества
3.2.1. Высокая согласованность между партиями — воспроизводимые результаты
Моноклональные антитела, полученные из гибридом, часто содержат загрязняющие легкие цепи и антитела из сыворотки. Присутствие этих примесей и нестандартный способ производства приводят к изменчивости от партии к партии и недостаточной воспроизводимости экспериментов.
Антитела REAfinity получены из определенной последовательности ДНК, которая кодирует только один тип тяжелой и легкой цепи, обеспечивая высокую чистоту антител (рис. 7). Они продуцируются в клетках млекопитающих в биологически и химически определенных, стандартизированных условиях культивирования, что приводит к высокой согласованности и чистоте партий по сравнению с моноклональными антителами мыши или крысы. Кроме того, каждая произведенная партия проходит тщательный аналитический, биохимический и клеточный анализ (рис. 8).
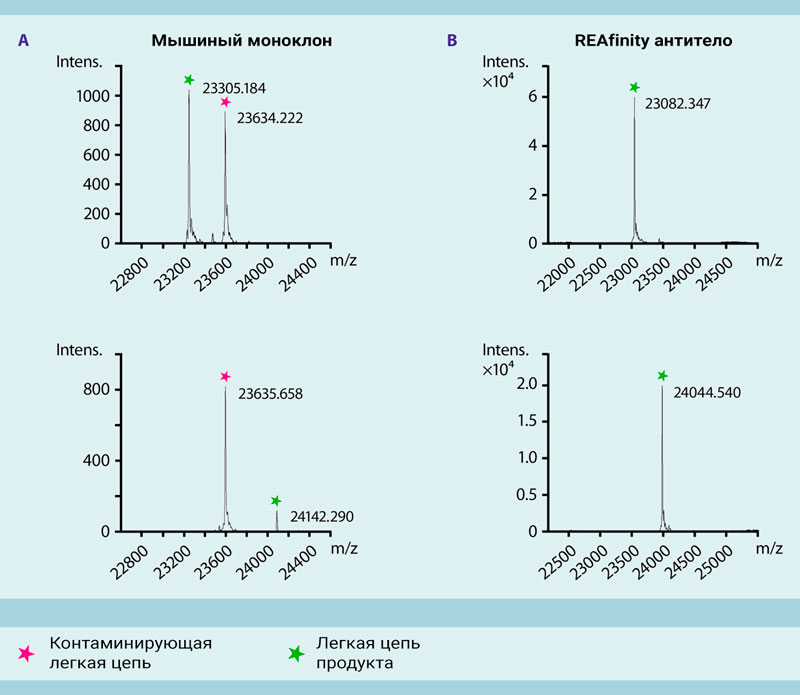
Рисунок 7: Масс-спектрометрический анализ очищенных антител показывает, что REAfinity антитела являются определенными продуктами, в то время как антитела из гибридомы могут представлять собой смесь.
(А) Масс-спектрометрический анализ двух примеров моноклональных антител из гибридомы показывает, что оба содержат вторую легкую цепь с молекулярной массой около 23, 635 Да. В одном примере (внизу слева) количество загрязняющей легкой цепи намного превышало легкую цепь продукта приблизительной массы 24, 142 Да.
(B) Два примера рекомбинантных антител REAfinity показывают чистые популяции легкой цепи.
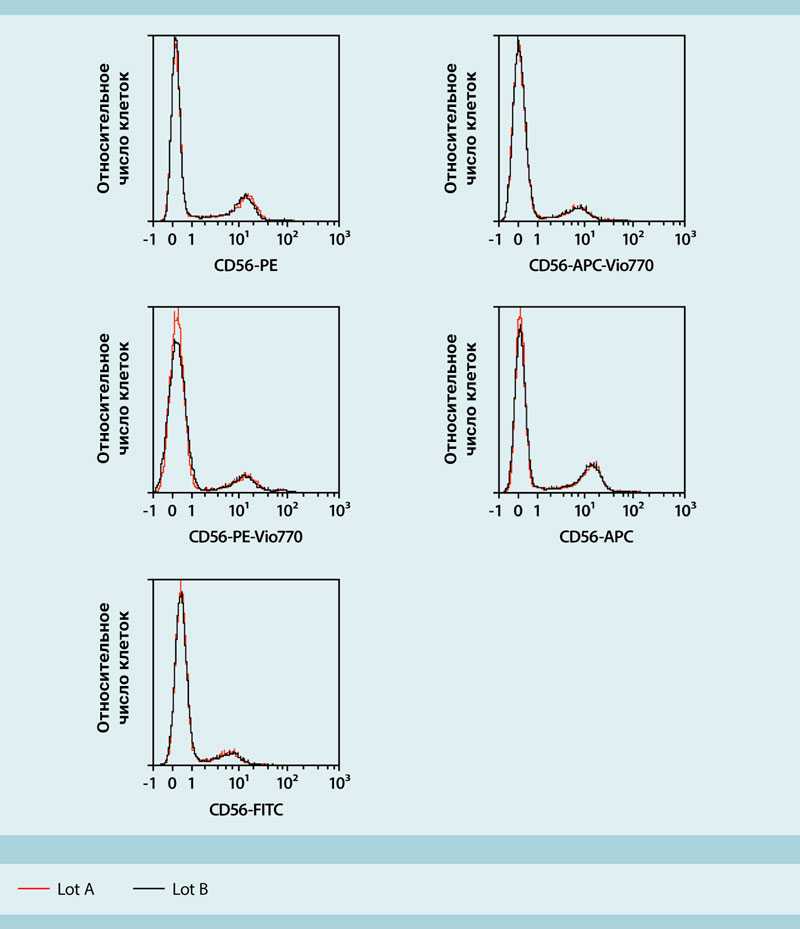
Рисунок 8: Эффективность окрашивания REAfinity антител практически одинакова для разных партий.
Две производственные партии из пяти различных конъюгатов (флуорохром- REAfinity антитело против CD56) сравнивали методом проточной цитометрии с использованием прибора MACSQuant® Analyzer. Две кривые гистограммы (черный и красный) представляют два лота (партии). При использовании мононуклеарных клеток периферической крови человека (РВМС) от одного донора эффективность окрашивания от партии к партии была практически одинаковой.
3.2.2. Отсутствие связывания с Fcγ-рецептором — снижение фонового сигнала
Высокие фоновые сигналы от антител часто ухудшают качество результатов проточной цитометрии. Одной из причин высоких фоновых сигналов является неспецифическое связывание антител с Fcγ-рецепторами на лейкоцитах. Чтобы избежать этого типа неспецифического связывания, во время окрашивания антителами используются блокирующие Fc-фрагмент реагенты. Однако процедура блокировки является трудоемкой и дорогостоящей.
Антитела REAfinity имеют мутированную область Fc от IgG1 человека, которая устраняет их связывание с рецепторами Fcγ (рис. 9). Это позволяет проводить фоновый анализ и устраняет необходимость в дополнительных этапах блокирования, таких как использование реагента, блокирующего FcR (рис. 10). Следовательно, протоколы окрашивания намного быстрее с антителами REAfinity (таблица 3).
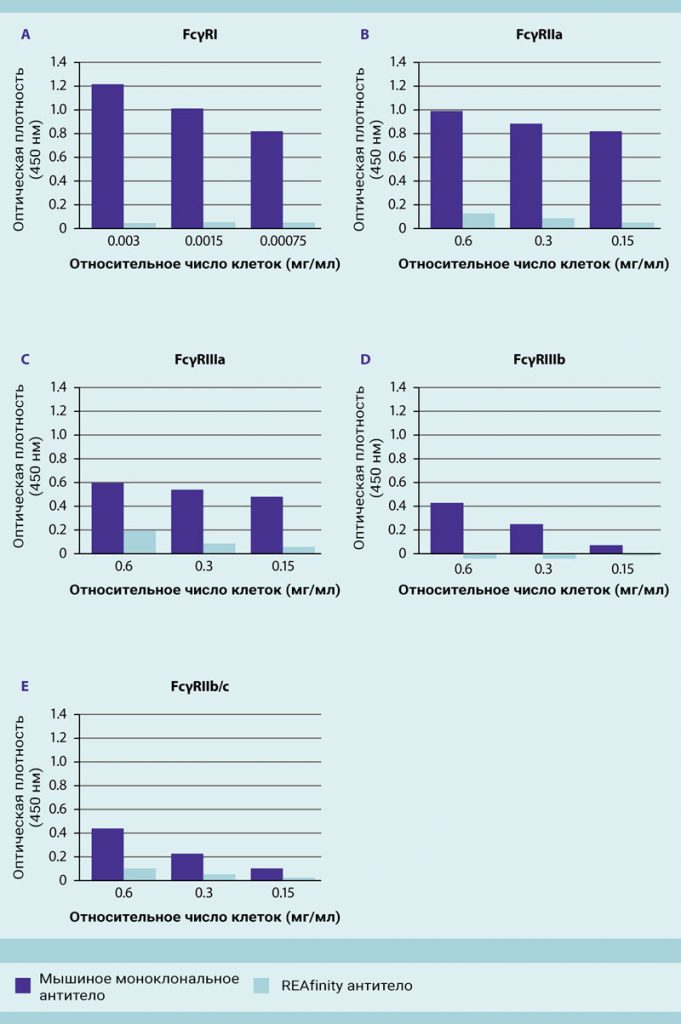
Рис.9: Рекомбинантно сконструированные антитела REAfinity не связываются с Fcγ-рецепторами.
CD144-специфичные мышиные моноклональные антитела (темно-фиолетовые столбики), полученные из гибридомы, связываются с высокоаффинными рецепторами FcγRI (CD64), а также с низкоаффинными FcγRIII (CD16) и FcγRII (CD32) рецепторами. Напротив, антитела REAfinity (светло-фиолетовые столбики) практически не взаимодействуют с Fcγ-рецепторами. Связывание с пятью клеточными Fcγ-рецепторами сравнивали, используя иммуноферментные анализы (ELISA).
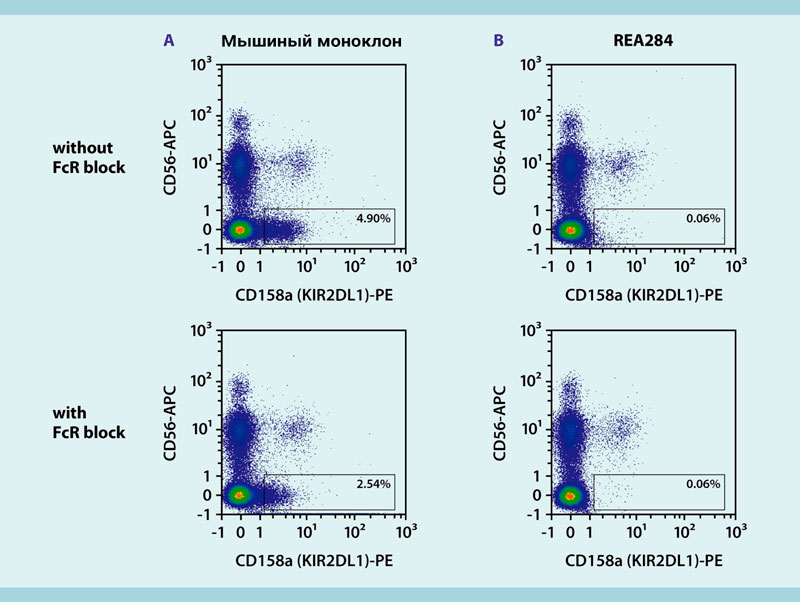
Рисунок 10: Окрашивание антителами REAfinity не показывает фонового сигнала, даже без блокирования FcR.
Мононуклеарные клетки перефирической крови (PBMCs) человека окрашивали либо конъюгатом фикоэритрина (PE) с мышиным моноклональным антителом к CD158a, либо конъюгатом фикоэритрина (PE) c антителом REAfinity к CD158a (клон: REA284). Окрашивание проводили без блокировки FcR (верхняя часть рисунка) и с блокировкой FcR (нижняя часть рисунка). Мышиное моноклональное антитело (A) неспецифично связывается с CD56-отрицательными клетками. Окрашивание антителом REAfinity (B) не показывает фонового сигнала. Клетки анализировали проточной цитометрией на приборе MACSQuant® Analyzer 10. Клеточный дебрис и мертвые клетки были исключены из анализа на основе сигналов рассеяния и флуоресценции пропидий йодида (PI).
Таблица 3: Протоколы окрашивания для иммунофенотипирования маркеров поверхности клеток человека и мыши
| Стадии процесса | Продолжительность каждого шага | |
| Антитела, полученные из гибридомы | REAfinity Антитела
|
|
| Подготовка 106 клеток | — | — |
| Добавление блокирующего реагента к клеткам и инкубирование при 4 ° С или комнатной температуре | 10-15 мин | — |
| Добавление первичных антител и инкубирование при 4 ° С или комнатной температуре | 10-30 мин | 10 мин |
| Промывание клеток | 1-2 раза каждый по 10 мин | 10 мин |
| Ресуспендирование и анализирование клеток | — | — |
| Общая процедура окрашивания | 30-65 мин | 20 мин |
3.2.3. Один универсальный изотип — простое планирование эксперимента
Все антитела REAfinity, то есть клоны REA, имеют один и тот же изотип IgG1 человека, что исключает необходимость включения многочисленных изотипических контролей во время анализа данных проточной цитометрии (рис. 11). Это дает возможность работать только с одной разновидностью изотипического контроля, снижая сложность планирования эксперимента и экономя время.
Напротив, моноклональные антитела, полученные из гибридомы, состоят из изотипов антител, полученных из разных видов, и, следовательно, требуют множественного контроля изотипа. Это усложняет не только управление запасами реагентов, но и дизайн панели при постановке экспериментов.
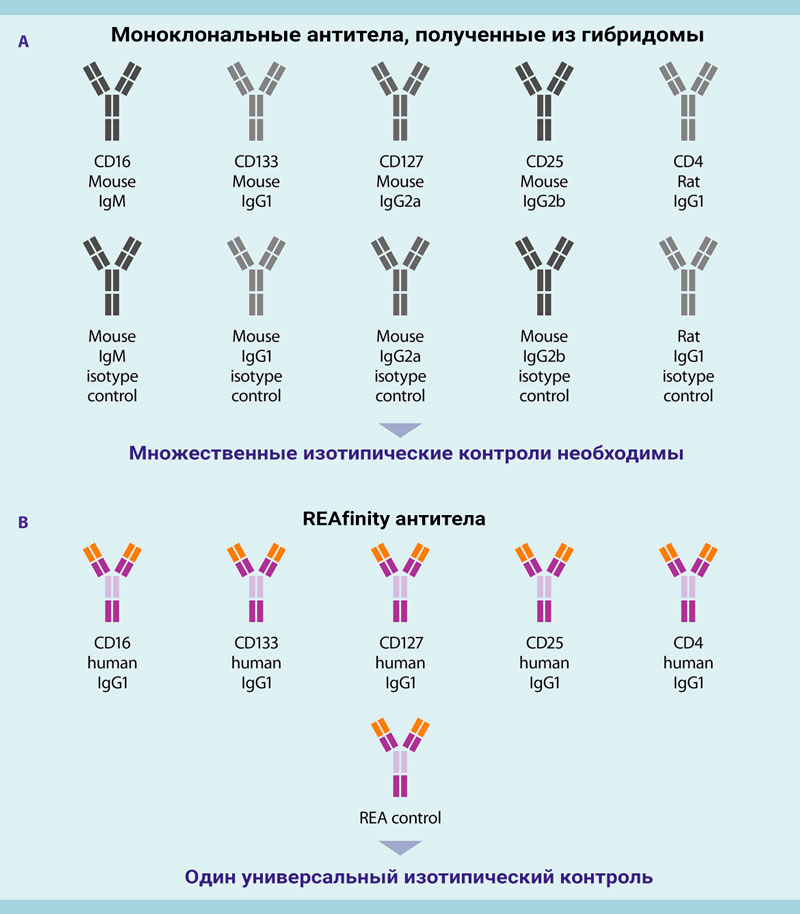
Рисунок 11: Простое планирование эксперимента только с одним изотипическим контролем для всех REAfinity антител.
Все антитела REAfinity, то есть клоны REA, имеют один и тот же изотип IgG1 человека, что исключает необходимость включения многочисленных изотипических контролей во время анализа данных проточной цитометрии.
Помимо этих уникальных свойств, все антитела REAfinity проходят строгие процессы контроля производства и качества. Для каждой специфичности применяется технология скрининга антител высшего качества для идентификации клона с самой высокой аффинностью и специфичностью. Только лучший кандидат отбирается, чтобы стать клоном рекомбинантно сконструированных антител (recombinantly engineered antibody; REA).
3.3. Рекомбинантные антитела REAfinity: оптимизированные под применение проточной цитометрии
Антитела REAfinity разработаны с учетом их применения в проточной цитометрии. Их высокая чистота, отсутствие фонового сигнала и стандартизированный процесс конъюгации с флуорохромом обеспечивают превосходные результаты в экспериментах с проточной цитометрией по сравнению с моноклональными антителами, полученными из гибридомы (рис. 12–14).
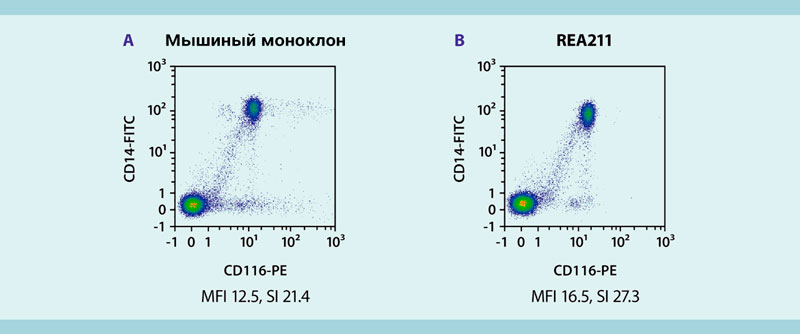
Рис. 12: Специфическое обнаружение человеческих CD116 + клеток с помощью клона REA 211.
Мононуклеарные клетки перефирической крови (PBMCs) человека окрашивали либо конъюгатом фикоэритрина (PE) с мышиным моноклональным антителом (A), распознающим CD116, либо конъюгатом фикоэритрина (PE) с REAfinity Antibody (B), распознающим CD116. Клетки также окрашивали конъюгатом изотиоцианата флуоресцеина (FITC) с антителом против CD14. Анализ с помощью проточной цитометрии выполняли на приборе MACSQuant Analyzer 10. Клеточный дебрис и мертвые клетки были исключены из анализа на основе сигналов рассеяния и флуоресценции пропидий йодида (PI).
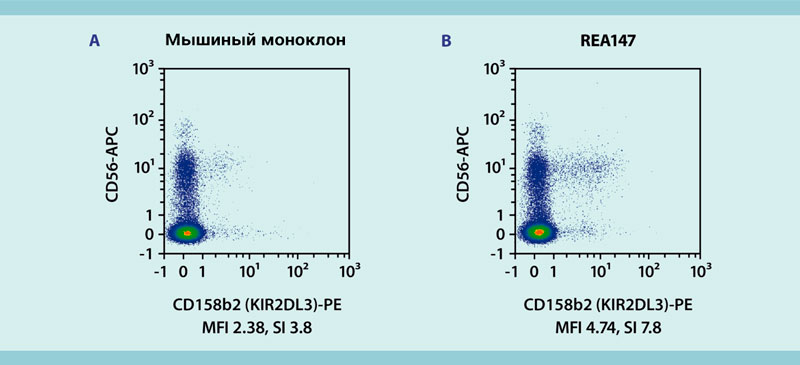
Рис. 13: Специфическое обнаружение клеток CD158b2 + человека с помощью клона REA147
Мононуклеарные клетки перефирической крови (PBMCs) человека окрашивали либо конъюгатом фикоэритрина (PE) с мышиным моноклональным антителом (A), распознающим CD158b2, либо конъюгатом фикоэритрина (PE) с REAfinity Antibody (B), распознающим CD158b2. Клетки также окрашивали конъюгатом флуорохрома APC с антителом против CD56 (клон: REA196). Анализ с помощью проточной цитометрии выполняли на приборе MACSQuant Analyzer 10. Клеточный дебрис и мертвые клетки были исключены из анализа на основе сигналов рассеяния и флуоресценции пропидий йодида (PI).
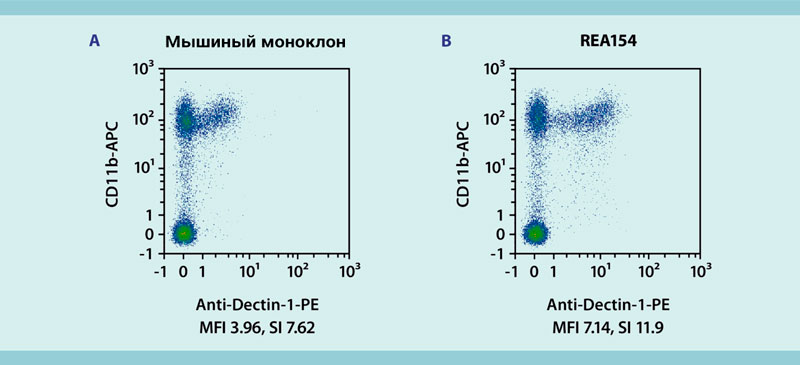
Рисунок 14: Специфическое обнаружение мышиных клеток (dectin-1 +) с клоном REA154.
Клетки костного мозга мышей BALB/c окрашивали либо либо конъюгатом фикоэритрина (PE) с мышиным моноклональным антителом (A), распознающим dectin-1 , либо конъюгатом фикоэритрина (PE) с REAfinity Antibody (B), распознающим dectin-1. Клетки также окрашивали конъюгатом флуорохрома APC с антителом против CD11b. Анализ с помощью проточной цитометрии выполняли на приборе MACSQuant Analyzer 10. Клеточный дебрис и мертвые клетки были исключены из анализа на основе сигналов рассеяния и флуоресценции пропидий йодида (PI).
3.4. Многоцветная проточная цитометрия с рекомбинантными антителами REAfinity.
Клоны REAfinity доступны с сотнями специфичностей и конъюгированы с различными флуорофорами для решения задач многоцветной проточной цитометрии. Текущие варианты включают традиционные красители, такие как FITC, PE, APC, и более новые версии, такие как Vio® и VioBright ™ Dyes (рис. 15). Антитела REAfinity, конъюгированные с флуорохромами Vio, являются мощными и надежными инструментами для анализа многоцветной цитометрии, что приводит к высокочувствительному, воспроизводимому и быстрому определению профиля клеток.
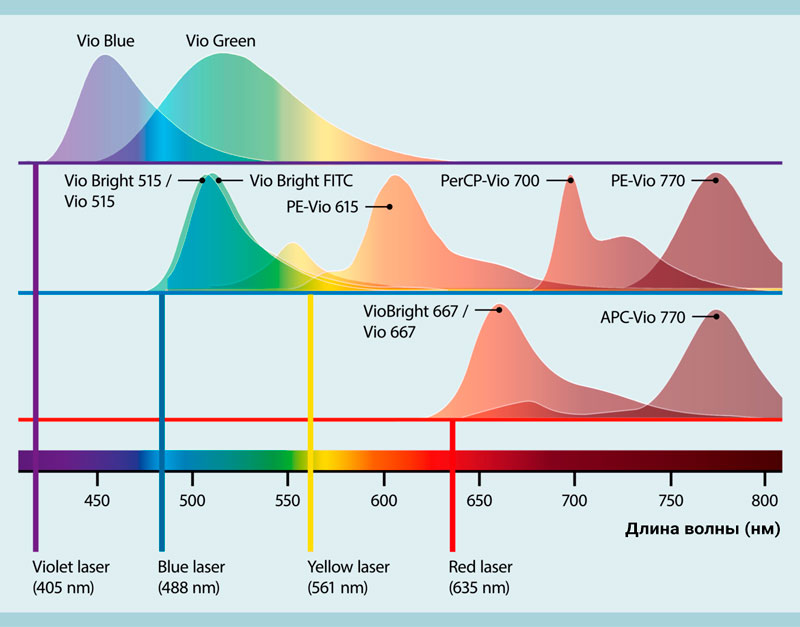
Рис.15. Спектры излучения флуорохромов VioBlue, VioBright 515, Vio 515, VioBright FITC, PE-Vio 615, PerCP-Vio 700, PE-Vio 770, VioBright 667, Vio 667 и APC-Vio 770, а также соответствующие длины волн лазера.

